Calore latente
Il calore latente è la quantità di calore necessaria per completare un cambiamento di stato fisico della materia, ossia per modificare lo stato di aggregazione molecolare in ogni parte di una sostanza.
Perché è detto latente? È detto latente in quanto lo scambio di calore non è rivelato da nessuna variazione di temperatura. Si verifica in condizioni isotermiche.
Il calore latente è pari alla differenza di energia cinetica delle particelle di un corpo tra lo stato fisico iniziale e quello finale.
Un esempio di calore latente
Quando l'acqua raggiunge la temperatura di ebollizione ( 100°C ) comincia un passaggio di stato fisico. L'acqua liquida si trasforma in vapore acqueo.
Tuttavia, la trasformazione non è istantanea in ogni parte del corpo.
Una parte dell'acqua resta allo stato liquido mentre un'altra parte evapora.
Fin quando tutta l'acqua non si è trasformata in vapore, la temperatura del liquido resta costante a 100°C.
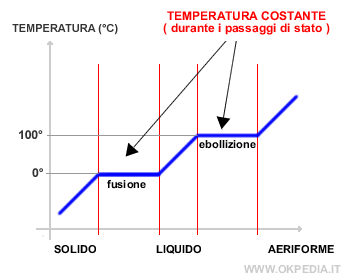
Continuando a fornire calore, la temperatura dell'acqua non cresce ulteriormente.
Il calore fornito a temperatura costante si chiama calore latente.
Il calore latente ceduto durante il passaggio di stato da liquido a aeriforme ( evaporazione ), viene poi riassorbito nella trasformazione inversa da aeriforme a liquido ( condensazione ).
Altro esempio. Nella fusione il calore latente è la quantità di calore necessaria per far passare la materia dallo stato solido allo stato liquido.
